CRISPR – O tehnologia medicala inovativa
CRISPR este o tehnologie revoluționară a edita precis și eficient secvențele de ADN. CRISPR vine de la numele din engleza: Clustered Regularly Interspaced Short Palindromic Repeats. Mai jos prezint câteva aspecte care fac aveasta tehnologie inovativă, ce metode au precedat-o, terapiile testate in prezent și statutul actual al tratamentelor bazate pe CRISPR.
De ce este CRISPR inovativ?
CRISPR este o tehnologie inovativa deoarece preint o inalta precizie și specificitate in editarea ADN-ului. CRISPR-Cas9 poate tăia ADN-ul într-o locație specifică determinată de o secvență ghid ARN (guide RNA). Comparativ cu tehnologiile anterioare, este mult mai precisă.
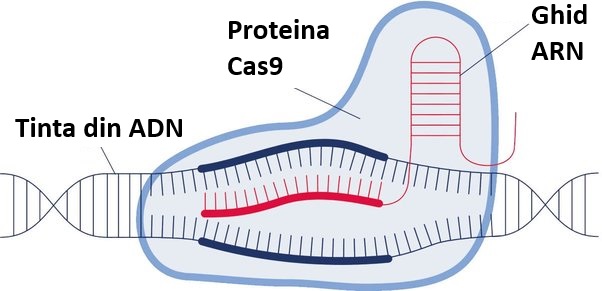
Aceasta tehnologie se poate folosi cu ușurință și este accesibila unor numar mare de cercetatori. Comparativ cu metodele mai vechi, CRISPR este mai simplu de proiectat și mai ieftin de utilizat, democratizând accesul la editarea genomică.
Tehnologia CRISPR are o mare versatilitate iar CRISPR poate fi utilizată pentru a dezactiva gene, introduce mutații punctiforme, insera gene sau modifica epigenetic expresia acestora. De asemenea are o aplicabilitate largă si funcționează în multiple organisme, inclusiv în celule umane, animale și vegetale.
Ce se folosea înainte de CRISPR?
Înainte ca tehnologia CRISPR să revoluționeze domeniul editării genetice, cercetătorii aveau la dispoziție mai multe tehnici de modificare a genomului, care, deși eficiente, erau mult mai complexe, costisitoare și mai puțin precise decât CRISPR. Printre cele mai importante tehnici utilizate se numără zinc finger nucleases (ZFNs) și transcription activator-like effector nucleases (TALENs).
1. Zinc Finger Nucleases (ZFNs)
Zinc Finger Nucleases sunt proteine fuzionate, formate dintr-o secvență de recunoaștere a ADN-ului (denumită „zinc finger”) și o nuclease capabilă să taie ADN-ul. Aceste proteine se leagă de o secvență specifică de ADN și creează o ruptură dublu-catenară, care poate fi reparată prin repararea naturii celulare (prin unirea capetelor sau recombinare omologă).
Deși ZFNs au fost un pas semnificativ în editarea genetică, ele aveau câteva limitări majore. Designul acestor proteine era complicat și necesita multă expertiză, iar eficiența în obținerea unor tăieturi precise și specifice era uneori scăzută. Totodată, ZFNs aveau o tendință mai mare de a produce efecte off-target (tăieturi nedorite în alte părți ale genomului), ceea ce le făcea mai riscante în aplicații clinice.
2. TALENs (Transcription Activator-Like Effector Nucleases)
TALENs sunt o altă tehnologie de editare genetică folosită înainte de CRISPR. Acestea sunt proteine care combină domenii care recunosc secvențe de ADN specifice (TAL effectors) cu o nuclease capabilă să taie ADN-ul. Deși TALENs sunt mai ușor de proiectat decât ZFNs și oferă o mai mare precizie în recunoașterea secvențelor țintă, acestea sunt totuși mai complexe și costisitoare decât CRISPR.
TALENs au fost folosite cu succes în mai multe domenii, inclusiv în ingineria genetică a plantelor și în terapii de corectare a unor mutații genetice. Cu toate acestea, procesul de creare a unor astfel de proteine poate fi consumator de timp, iar costurile rămân semnificative.
3. Alte tehnici pre-CRISPR
Înainte de aceste tehnologii avansate, cercetătorii se foloseau de metode tradiționale de mutagenizare și recombinare genetică pentru a modifica ADN-ul, de obicei prin utilizarea agenților chimici sau radiațiilor pentru a induce mutații aleatorii. De asemenea, unele tehnici mai timpurii, cum ar fi inserarea de plasmide sau virusuri modificate genetic, au fost folosite pentru a introduce secvențe de ADN în celule sau organisme.
Tehnologiile anterioare CRISPR, cum ar fi ZFNs și TALENs, au avut un impact semnificativ asupra domeniului biotehnologic și genetic, dar erau mult mai complexe și mai puțin precise decât CRISPR. Lansarea CRISPR în 2012 a simplificat dramatic procesul de editare genetică, făcându-l accesibil mai larg, mult mai rapid și mult mai precis, ceea ce a deschis noi orizonturi pentru cercetare și aplicații clinice, inclusiv terapii genetice personalizate.
Terapii care folosesc CRISPR
- Boli genetice precum Beta-talasemia și anemia falciformă (Sickle Cell Disease): Terapia aceasta ex vivo Casgevy, adica modificarea celulelor stem hematopoietice ale pacientului și reintroducerea acestora, a arătat rezultate promițătoare.
- Cancer: Editarea celulelor T pentru a îmbunătăți recunoașterea tumorilor. De exemplu, în studiile clinice, CRISPR a fost utilizată pentru a modifica celulele T în combaterea melanomului, a cancerului pulmonar și a mielomului multiplu.
- Bolile oftalmologice: Editarea genelor pentru tratamentul Leber Congenital Amaurosis 10 (o formă rară de orbire genetică).
- Bolile infecțioase: Cercetările explorează CRISPR pentru tratarea infecției HIV, prin eliminarea ADN-ului viral din celulele infectate.
Stadiul actual al terapiilor CRISPR:
1. Terapii aprobate de autorități
Beta-talasemia și anemia falciformă
Casgevy™ (Exagamglogene autotemcel): Această terapie a primit aprobarea Agentiei Europene a Medicamenului pentru tratamentul bolii celulare secvențiale (SCD) la pacienții cu vârsta de 12 ani și peste. Terapia presupune editarea celulelor stem din sângele pacientului pentru a crește producția de hemoglobină fetală, ceea ce poate reduce sau elimina episoadele dureroase asociate cu SCD.
2. Terapii în stadiu clinic
Mai multe terapii bazate pe CRISPR sunt în prezent în studii clinice, unele dintre acestea arătând rezultate promițătoare pentru tratamentele bolilor genetice și chiar cancerului. Iată câteva exemple:
- NTLA-2001: Dezvoltată de Intellia Therapeutics și Regeneron, această terapie vizează tratarea cardiomiopatiei amiloidozice familiale, o afecțiune cauzată de mutații ale genei transtiretinei. Terapia utilizează CRISPR pentru a edita gena responsabilă de producerea proteinelor amiloide care cauzează daune inimii și altor organe. Este în prezent în faza III a studiilor clinice.
- CTX-110: Această terapie este investigată pentru posibile aplicații în tratamentul cancerului, în special pentru modificarea celulelor imunitare care pot combate tumori. Se află în faza II a studiilor clinice.
În plus, există studii în desfășurare care folosesc CRISPR pentru tratarea infecțiilor bacteriene cronice (de exemplu, infecțiile tractului urinar) și a altor tulburări genetice
Premiul Nobel pentru Chimie in 2020 acordat pentru CRIPSR
CRISPR a fost recunoscut cu Premiul Nobel pentru Chimie în 2020, acordat cercetătoarelor Emmanuelle Charpentier și Jennifer Doudna. Ele au fost premiate pentru descoperirea și dezvoltarea metodei CRISPR-Cas9 ca un instrument de editare a genomului.

În 2012, Charpentier și Doudna au demonstrat cum sistemul natural CRISPR-Cas9, folosit de bacterii pentru a se apăra împotriva virusurilor, poate fi adaptat pentru a tăia ADN-ul în locații precise în orice organism.
Aceasta a revoluționat biologia moleculară, fiind folosită în cercetare fundamentală, medicină, agricultură și biotehnologie. Premiul Nobel a subliniat potențialul enorm al CRISPR de a transforma terapiile genetice și alte domenii.
Perspective CRISPR
CRISPR are un potențial enorm și continuă să fie explorat pentru terapii inovative, inclusiv în boli poligenice, îmbunătățirea culturilor agricole și biologia sintetică. Totuși, provocările etice și de siguranță (ex. efectele off-target) rămân subiecte majore de cercetare și dezbatere.